

香港中文大學(中大)今日(24日)公布,中大生命科學學院助理教授周熙文教授領導的研究團隊研發(fā)了一套基於大數(shù)據(jù)的生物信息分析流程,有助識別人類腦部變異神經(jīng)元的特徵和生物標記,證實重新進入細胞周期的神經(jīng)元對阿茲海默癥及相關腦退化癥的發(fā)病和疾病進展有重大影響。這項發(fā)現(xiàn)可為研發(fā)腦退化癥精準醫(yī)療提供新方向。有關研究結果最近發(fā)表在國際知名期刊《PLOS Biology》上,並入選為期刊焦點文章。
細胞周期是指細胞持續(xù)分裂、生長再到下次分裂的循環(huán)過程,而在此過程中細胞也在不斷老化,直至被新生的細胞取代。與一般細胞不同,神經(jīng)元在大腦發(fā)育成熟後便會停止分裂,無法再生。周熙文教授早前的研究提出,部分神經(jīng)元在承受不同壓力的刺激下會重新啟動細胞周期機器,但受研究方法所限,難以精準及客觀地預測它們被激活後的變化。
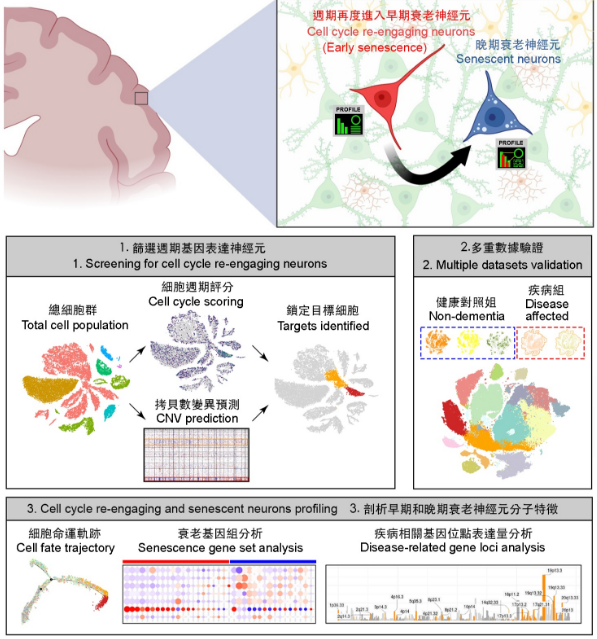
中大研究團隊利用嶄新的生物信息分析流程辨別衰老神經(jīng)元處於細胞周期的表徵及與疾病相關基因的關係。
由於這些變異細胞在整個大腦中的分布難以預測且密度相對較低,傳統(tǒng)組織學或大塊組織轉(zhuǎn)錄組測序技術等研究方法,均無法識別這些細胞的分子特徵、衍生過程和原因,以及它們對周邊細胞的影響。此外,傳統(tǒng)實驗手段也無法分辨這些衰老神經(jīng)元是否會因大腦微環(huán)境的多樣性而出現(xiàn)任何疾病的特異性。
周熙文研究團隊建基於神經(jīng)元的細胞生物學特異性,定制了一套生物信息分析流程,可用於進行多腦單核轉(zhuǎn)錄組數(shù)據(jù)的統(tǒng)合分析。團隊利用了多國阿茲海默癥人腦轉(zhuǎn)錄組和病人臨床數(shù)據(jù)進行分析,通過RNA定序找到細胞周期不同階段的特定標誌物,顯示細胞核處於循環(huán)中的哪個階段,以至其衰老功能改變的特徵。他們發(fā)現(xiàn)神經(jīng)元再度啟動細胞周期機器後,並沒有繼續(xù)完成分裂以產(chǎn)生子代神經(jīng)元,反而是激活了細胞衰老機制,導致衰老神經(jīng)元累積,從而影響大腦整體功能及穩(wěn)態(tài)。
周熙文表示,研究發(fā)現(xiàn)這些重新進入細胞周期的衰老神經(jīng)元更多出現(xiàn)在阿茲海默癥患者身上,並導致多個該癥風險因素相關的基因表達水平上升。同樣地,柏金遜癥和路易氏體失智癥患者大腦中亦有較多重新進入細胞周期的神經(jīng)元,數(shù)量明顯比健康大腦多。利用這種新的生物信息學分析流程,可更深入了解這些細胞的內(nèi)在特性,以及在疾病條件下所出現(xiàn)的特異性,以協(xié)助相關精準醫(yī)學的發(fā)展。
團隊以阿茲海默癥作為研究模型,分析結果均發(fā)現(xiàn)衰老神經(jīng)元普遍處於功能障礙狀態(tài),與周邊正常的神經(jīng)元截然不同。在健康的大腦中,這些處於初期及晚期衰老神經(jīng)元在正常的器官穩(wěn)態(tài)調(diào)控下的數(shù)量得以控制。然而,在阿茲海默癥影響下,衰老神經(jīng)元會累積,更會特異地表達一系列促進發(fā)炎反應的標記物、代謝功能失調(diào)及與病理相關的分子特徵。
此外,研究團隊進一步利用了柏金遜癥和路易體失智癥模型和小鼠大腦老化模型進行分析,驗證這種大數(shù)據(jù)分析方法對不同疾病模型和跨物種數(shù)據(jù)的廣泛應用性,為衰老神經(jīng)元在大腦老化和疾病發(fā)病機制中的作用研究提供了新的見解,補充了傳統(tǒng)實驗手段的不足。而分析所揭示的疾病特異性分子特徵亦可為未來診斷和抗衰老治療策略的開發(fā)帶來新方向。
這項研究的其他重要貢獻者包括中大生命科學學院博士後研究員吳鄧博士和博士生孫嘉莉。
頂圖:(右起)周熙文教授、孫嘉莉女士及吳鄧博士。




